业务咨询
神经保护
一、实验目的
衰老是生物体渐进性损伤累积和功能退化的过程,最终导致环境适应能力下降、疾病易感和死亡风险增加。因此,衰老是许多与年龄相关疾病病的主要风险因素。生物的衰老进程涉及诸多病理、生理因素,具有渐进性、阶段性、复杂性和多样性特点。从整体动物表型层面来看,衰老的主要特征包括抗胁迫能力下降、机体功能减退、退行性疾病发生率增大、死亡风险升高等。López-Otín等科学家最近提出了衰老的十二个主要特征,包括基因组不稳定、端粒消耗、表观遗传改变、蛋白稳态失衡、巨噬细胞功能丧失、营养感知失调、线粒体功能障碍、细胞衰老、干细胞衰竭、细胞间通讯改变、慢性炎症和菌群失调。秀丽隐杆线虫具有生命周期短、遗传资源丰富、关键信号通路与人类高度同源、实验操作与维护简单等优点,已成为探寻衰老相关机制、构建衰老相关模型的强有力模型。该测试项目评价样品对线虫寿命的影响,评价其抗衰老的功效。
二、建模原理
自然寿命及运动能力实验不需要建模处理。
氧化应激实验:百草枯能够高效诱导线虫体内产生大量活性氧(ROS),从而模拟氧化应激的病理状态。
ASH神经元存活实验及避化实验:HA759线虫模型{rtIs11 [osm-10p::GFP + osm-10p::HtnQ150 + dpy-20(+)]}:在ASH神经元中表达GFP和polyQ150,导致随发育出现进行性ASH神经元死亡(荧光点消失),使其调控的对高渗溶液的识别及回避能力消失。
趋化实验:CL2355线虫模型{dvIs50 [pCL45 (snb-1::Abeta 1-42::3' UTR(long) + mtl-2::GFP] I}:经高温诱导后在神经元细胞中表达Aβ1-42,使神经元损伤甚至死亡,导致感官趋化性、联想学习能力缺陷。CL2122线虫模型{dvIs15 [(pPD30.38) unc-54(vector) + (pCL26) mtl-2::GFP]}:为相同启动子敲入的线虫,但不表达Aβ1-42,为CL2355的对照。
三、实验方案
3.1 最大检测浓度摸索
①实验动物:同步化的L4期野生型N2线虫。
②实验分组:对照组、每个样品6个剂量组(1个样品),共6组。
③实验方法:将L4期野生型N2线虫转移到按表1体系配制的96孔板中,孔板中AMP的终浓度为100 μg/mL、5-FUdR的终浓度为75 μg/mL以及NA22的终浓度约为0.6(OD 570 nm)。在20 ℃、120 rpm条件下培养48 h以后,在倒置显微镜下观察并记录线虫是否存在大量死亡的现象。每组线虫数量不少于30条。
表1 MTC实验培养体系
组别 | 浓度 | Vsample (μL) | VNA22 (μL) | V5-FUdR (μL) | VAMP (μL) | Vworms (μL) | VS Medium (μL) |
对照组 | 0 | 0 | 10 | 1.5 | 2 | 20 | 66.5 |
样品组 | a mg/mL | b | 10 | 1.5 | 2 | 20 | 66.5-b |
3.2 样品对自然寿命的影响
①实验动物:同步化的L4期野生型N2线虫。
②实验分组:对照组、每个样品4个剂量组(1个样品),共5组。
③实验方法:移取同步化的L4期野生型N2线虫到按表1体系配置的96孔板(每孔总体积100 μL)中。孔板中AMP的终浓度为100 μg/mL、5-FUdR的终浓度为75 μg/mL以及NA22的终浓度约为0.65(OD 570 nm),控制每孔10-20条线虫,每组设置6个复孔。在20 ℃、120 rpm条件下培养,从给药开始记作第0天,从第10天开始进行线虫存活计数,往后每隔1天对线虫存活状况进行统计,直至线虫全部死亡。
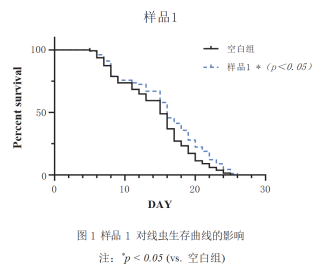
④检测指标:绘制线虫生存曲线,计算平均寿命、中位寿命和最大寿命的延长率。
⑤生存曲线示例图:
3.3 样品对百草枯氧化存活的影响
①实验动物:同步化的L4期野生型N2线虫。
②实验分组:对照组、每个样品4个剂量组(1个样品),共5组。
③实验方法:移取同步化的L4期野生型N2线虫到按表1体系配置的96孔板(每孔总体积100 μL)中。孔板中AMP的终浓度为100 μg/mL、5-FUdR的终浓度为75 μg/mL以及NA22的终浓度约为0.5(OD 570 nm),控制每孔10-15条线虫加入到孔板中,每组设置6个复孔。在20 ℃、120 rpm条件下培养24 h后,向每组中加入终浓度为50 mM的百草枯溶液进行造模处理,继续在20 ℃、120 rpm条件下培养。此时对秀丽线虫计数,此后每12 h进行一次计数,直至线虫全部死亡。
④检测指标:百草枯氧化存活。
3.4 样品对运动能力的影响
①实验动物:同步化的L4期野生型N2线虫。
②实验分组:对照组、每个样品4个剂量组(1个样品),共5组。
③实验方法:移取同步化的L4期野生型N2线虫到按表2体系配置的48孔板(每孔总体积500 μL)中。孔板中AMP的终浓度为100 μg/mL、5-FUdR的终浓度为75 μg/mL以及NA22的终浓度约为0.6(OD 570 nm),控制每孔200-300条线虫加入到孔板中,每组设置3个复孔。在20 ℃、120 rpm条件下培养至第10天,收集并清洗线虫。移取20 μL虫液滴于预先准备好的3.5 cm NGM板上,录制30 s线虫爬行分析视频,再重新移取50 μL虫液(大概5-10条线虫),滴于载玻片上,录制30 s游动分析视频。采用Matlab、Image J和用Tierpsy Tracker等软件量化获取线虫的平均爬行速度、游动速度、身体摆动频率等指标。
表2 运动能力实验培养体系
组别 | 浓度 | Vsample (μL) | VNA22 (μL) | V5-FUdR (μL) | VAMP (μL) | Vworms (μL) | VS Medium (μL) |
对照组 | 0 | 0 | 50 | 7.5 | 10 | 100 | 332.5 |
样品组 | x mg/mL | y | 50 | 7.5 | 10 | 100 | 332.5-y |
④检测指标:平均爬行速度、游动速度、身体摆动频率等。
3.5 ASH神经元实验最大检测浓度摸索
①实验动物:同步化的L1期HA759线虫。
②实验分组:对照组、每个样品5个剂量组(1个样品),共6组。
③实验方法:将L1期HA759线虫转移到按表3体系配制的96孔板中,在15 ℃、120 rpm条件下培养48 h以后,在倒置显微镜下观察并记录线虫是否存在大量死亡的现象。每组线虫数量不少于30条。
表3 ASH神经元实验MTC实验培养体系
组别 | 浓度 | Vsample (μL) | VNA22 (μL) | Vworms (μL) | VS Medium (μL) |
对照组 | 0 | 0 | 10 | 20 | 70 |
样品组 | a mg/mL | b | 10 | 20 | 70-b |
3.6 样品对神经元存活的影响
①实验动物:同步化的L1期HA759线虫。
②实验分组:对照组、每个样品4个剂量组(1个样品),共5组。
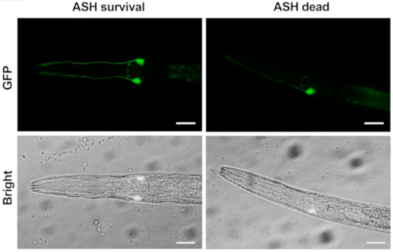
③实验方法:移取同步化的L1期HA759线虫到按表4体系配置的48孔板(每孔总体积500 μL)中。孔板中NA22的终浓度约为0.6(OD 570 nm),控制每孔200-300条线虫加入到孔板中,每组设置3个复孔。在15 ℃、120 rpm条件下培养72 h,收集并清洗线虫。用左旋咪唑麻醉后在荧光显微镜下成像,记录ASH神经元存活情况,2点荧光记为存活,1点荧光和0点荧光均为死亡。计算ASH神经元存活率。
表4神经元存活实验培养体系
组别 | 浓度 | Vsample (μL) | VNA22 (μL) | Vworms (μL) | VS Medium (μL) |
对照组 | 0 | 0 | 50 | 100 | 350 |
样品组 | x mg/mL | y | 50 | 100 | 350-y |
④检测指标:ASH神经元存活率。
⑤ASH神经元存活示例图:
3.7 样品对避化率的影响
①实验动物:同步化L1期HA759线虫。
②实验分组:对照组、每个样品4个剂量组(1个样品),共5组。
③实验方法:移取同步化的L1期HA759线虫到按表4体系配置的48孔板(每孔总体积500 μL)中。孔板中NA22的终浓度约为0.6(OD 570 nm),控制每孔200-300条线虫加入到孔板中,每组设置3个复孔。在15 ℃、120 rpm培养72 h后,收集并清洗线虫。将检测用平板用30 µl 8 M的高渗甘油线均分为正常侧(N)和引诱剂侧(T)两个区域;并在T区域内、距离甘油线1 cm的位置平行滴加20 µl(200mM)的NaN3线,用以麻醉越过甘油线区域的线虫。将线虫均匀分散的滴加于N侧区域的中间部位;待线虫自由爬出缓冲液液滴后,在T区域距离边缘1 cm的位置滴加2 µl线虫引诱剂-双乙酰溶液,即刻盖住平板盖子,并将测试平板置于23 ℃恒温培养箱中放置90 min,待线虫爬开分散于平板两侧后,显微镜下统计甘油线两侧区域的线虫数量,并分别计数为N和T。并计算避化率。
避化率(%)= N/(T+N)
④检测指标:避化率。
⑤实验示意图:
3.8 趋化检测实验最大检测浓度摸索
①实验动物:同步化虫卵16 ℃恒温摇床培养36 h获得L1期CL2355线虫和CL2122线虫。
②实验分组:对照组、每个样品5个剂量组(1个样品),共6组。
③实验方法:将L1期CL2355线虫转移到按表3体系配制的96孔板中,在16 ℃、120 rpm条件下培养12 h后升温至23 ℃继续培养36 h,在倒置显微镜下观察并记录线虫是否存在大量死亡的现象。每组线虫数量不少于30条。
3.9 样品对趋化率的影响
①实验动物:同步化虫卵16 ℃恒温摇床培养36 h获得L1期CL2355线虫和CL2122线虫。
②实验分组:对照组、每个样品4个剂量组(1个样品),共5组。
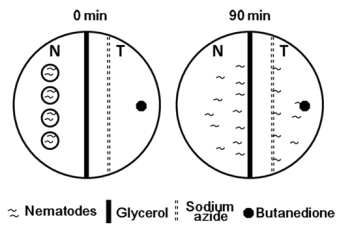
③实验方法:移取同步化的L1期CL2355线虫和CL2122线虫(对照组线虫)到按表4体系配置的48孔板(每孔总体积500 μL)中。孔板中NA22的终浓度约为0.6(OD 570 nm),控制每孔200-300条线虫加入到孔板中,每组设置3个复孔。在16 ℃、120 rpm恒温摇床培养12 h后升温至23 ℃,继续培养48 h,收集并清洗线虫。将检测用平板均分为正常侧(N)和引诱剂侧(T)两个区域。在N侧区域距离边缘1 cm的位置滴加1 µl无水乙醇和1 µl NaN3(200mM);之后在对应的T侧区域距离边缘1 cm的位置滴加1 µl线虫引诱剂-苯甲醛和1 µl NaN3(200mM);即刻盖住平板盖子,并将测试平板置于23ºC恒温培养箱中放置60 min,待线虫爬开分散于平板两侧后,显微镜下统计两侧区域的线虫数量,并分别计数为N和T,计算趋化率。
趋化率(%)=(T-N)/(T+N)
当线虫的神经元受损后,其对苯甲醛和乙醇的趋向性几率是相同的,因此,分布在N侧区域的线虫仅代表一半神经元受损线虫数,在T侧区域会等比例分布神经元损伤的线虫,通过(T-N)来统计神经元未损伤的线虫数,以消除误差。
④检测指标:趋化率。
⑤实验示意图: